Índice
| 1. | Introducción |
| 2. | Antecedentes científicos e históricos |
| 3. | Aplicaciones actuales y futuras del UPT |
| 4. | Discusión |
| 5. | Referencias |
- Introducción
Los avances de las técnicas analíticas continúan alertándonos sobre la presencia de un número cada vez mayor de sustancias insospechadas en materiales en contacto con alimentos. Estos productos químicos incluyen productos no deseados de reacciones, impurezas, metabolitos y/o productos de degradación. Además, hay una gran cantidad de sustancias en contacto con los alimentos que, si bien son conocidas, no han sido evaluadas previamente. La evaluación de estas sustancias requiere una gran cantidad de datos toxicológicos, lo que plantea un desafío tanto a nivel experimental como financiero. Con el fin de resolver este problema, durante los últimos 30 años se ha invertido grandes esfuerzos en desarrollar de los conceptos de umbral. Estos conceptos se basan en asumir que se puede establecer el umbral de exposición en valores por debajo de los cuales la probabilidad de efectos adversos para la salud es muy baja. Evalúan la toxicidad de un producto químico en base a los datos de toxicidad de sustancias químicas estructuralmente relacionadas. Si bien conocer la estructura química y los datos de exposición es indispensable para aplicar el concepto de umbral, éste puede ser utilizado para asignar riesgos a sustancias en ausencia de datos toxicológicos apropiados.
El presente informe revisa las normas del TOR de los EE.UU como un primer ejemplo de aplicación legal de los conceptos de umbral. Además, detalla cómo se desarrolló el concepto de Umbral de Preocupación Toxicológica (UPT) para evaluar y priorizar las sustancias desconocidas o no evaluadas hasta ahora. Por último, el informe reconsidera algunos de los temas más urgentes, poniendo en evidencia la necesidad de mayor investigación y debate.
- Antecedentes científicos e históricos
En los EE.UU., la Administración de Alimentos y Medicamentos (Food & Drugs Administration, FDA) introdujo en 1995 el concepto de Umbral de Regulación (Threshold of Regulation, TOR) para los aditivos alimentarios indirectos (21 C.F.R. §170.39). Basándose en el principio de minimis, esta norma exime a las sustancias de estar registradas como aditivos alimentarios si migran desde el envasado a los alimentos a niveles por debajo de un umbral de 0,5 ppb. Suponiendo una ingesta diaria de alimentos de 1,5 kg de líquidos y 1,5 kg de alimentos sólidos, el nivel de exposición en la dieta para los compuestos exentos de regulación por la normativa del TOR se fijó en <1,5 µg/persona/día.
Los compuestos cancerígenos o presuntos cancerígenos están excluidos de la exención de la regulación TOR, porque la carcinogenicidad se considera el parámetro toxicológico más sensible. Para calcular el valor umbral de 0,5 ppb, la potencia carcinogénica de varios cientos de sustancias químicas por vía oral probadas en roedores, fueron extrapoladas linealmente a concentraciones que representan un riesgo socialmente aceptable de uno por millón de desarrollo de tumores en humanos. Por lo tanto, el concepto se basa en un enfoque probabilístico y pretende proteger contra productos químicos no probados potencialmente cancerígenos [1].
Poco después de que EE.UU. introdujera el término TOR, un grupo de científicos y consultores de la industria publicó otro concepto de umbral, el UPT [2]. En lugar de establecer un único umbral, el UPT diferencia además entre las estructuras químicas y proporciona umbrales escalonados para sustancias con diferentes niveles de preocupación toxicológica (tabla 1). En 1978, Cramer y colaboradores. desarrollaron un árbol de decisión que asigna los productos químicos a las clases Cramer I-III en función de su importancia toxicológica estimada [ 3 ]. En 1996, Munro y colaboradores clasificaron 613 productos químicos no carcinógenos en las clases Cramer, mediante la aplicación de este árbol de decisión [ 2 ]. Posteriormente, establecieron los umbrales específicos para las tres clases de Cramer basándose en los datos toxicológicos existentes de estos productos químicos (Tabla 1). Munro y col. establecieron que las sustancias carcinógenas genotóxicas no deben evaluarse utilizando el enfoque UPT. En el año 2000, Kroes y su equipo confirmaron que la carcinogenicidad fue la variable más sensible y que el umbral general del 1,5 µg/persona/día protege suficientemente contra el cáncer [ 4 ]. En conformidad con un seminario de trabajo para expertos convocado por el International Life Sciences Institute (Instituto Internacional de Ciencias de la Vida, ILSI) Europa en 2003, Kroes y col. introdujeron dos nuevos niveles de umbral [ 5 ]. Establecieron un umbral de exposición de 0,15 µg/persona/día para los carcinógenos genotóxicos, por extrapolación lineal a bajas dosis, permitiendo de este modo la evaluación de genotóxicos en el marco del concepto UPT. Dicho límite solo excluyó algunos grupos de genotóxicos muy potentes, así como los carcinógenos no genotóxicos [5]. Además, se asignó un umbral más bajo a ciertos neurotóxicos y pesticidas (organofosfatos y carbamatos), debido a que los investigadores llegaron a la conclusión de que la neurotoxicidad no estaba suficientemente cubierta por el umbral para compuestos de la clase III de Cramer.
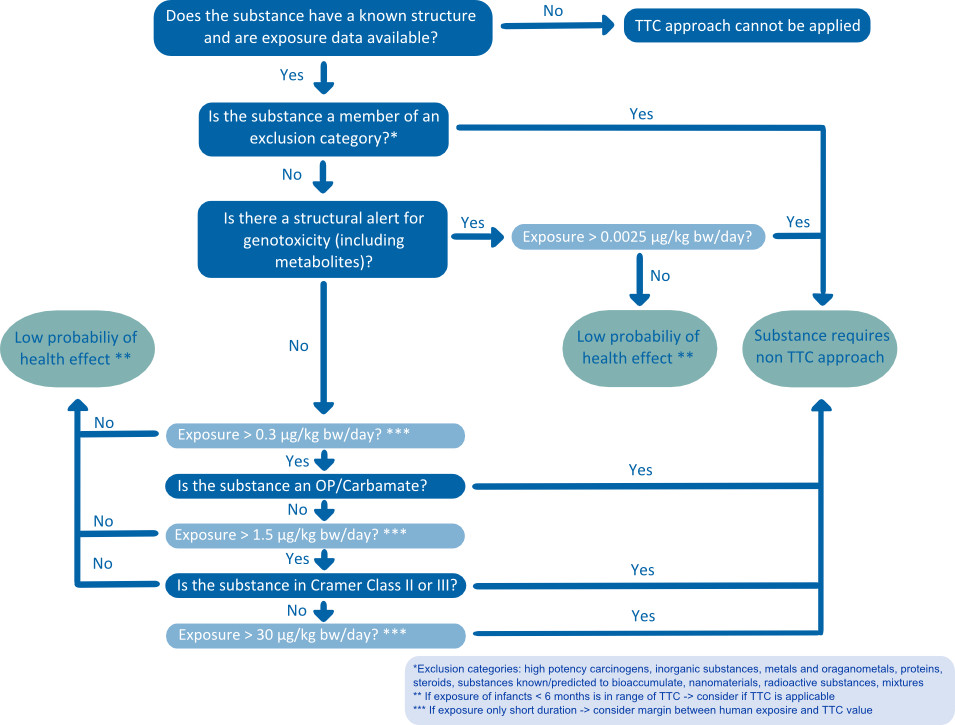
En 2012, la Autoridad Europea de Seguridad Alimentaria (EFSA) publicó un dictamen científico que establecía «que el UPT puede ser recomendado como una herramienta de detección útil, ya sea para el establecimiento de prioridades o para decidir si la exposición a una sustancia es tan baja que la probabilidad de los efectos nocivos efectos es pequeña y que no son necesarios más datos «[6]. De forma general, el trabajo de la EFSA acepta el árbol de decisión de Kroes [4], pero exigió varias mejoras de mayor o menor importancia (Figura 1). Entre ellas se incluye la eliminación de la clase II de Cramer, la revisión y el perfeccionamiento del árbol de decisión de Cramer basado en datos toxicológicos actuales y la evaluación de los agentes carcinógenos basada en el margen de exposición en lugar de en la extrapolación lineal a bajas dosis.
Tabla 1. Clasificación de umbrales y valores correspondientes
| Clasificación | TTC (µg/persona/d) | Referencia |
| Cramer class I | 1800 | Munro 1996 [2]* |
| Cramer class II | 540 | Munro 1996 [2]* |
| Cramer class III | 90 | Munro 1996 [2]* |
| Organofosfatos y carbamatos | 18 | Kroes 2004 [5]* |
| Carcinógenos | 1.5 | TOR rule, Rulis [1]** |
| Sustancias genotóxicas ( compuestos azoicos o N-nitrosos tipo aflatoxinas) | 0.15 | Kroes 2004[5]** |
* Los umbrales se calcularon en base a las curvas de distribución acumulada NOEL de experimentos con animales para cada clase estructural. El percentil 5 NOEL se transformó en un umbral de exposición humana mediante la aplicación de un factor de seguridad de 100, suponiendo un peso estándar de 60 kg. ** Los umbrales para los carcinógenos se obtuvieron de la extrapolación lineal de los valores TD50 a partir de experimentos en animales, con un riesgo de uno por millón para el desarrollo de tumores en humanos.
- Aplicaciones actuales y futuras del UPT
En el dictamen científico de la EFSA sobre el UPT se discutió la aplicación del concepto de sustancias en contacto con alimentos, aromatizantes, enzimas y coadyuvantes. Las migraciones de bajo nivel, las impurezas y los productos secundarios se consideraron también sustancias susceptibles de evaluación con el UPT. No está claro si estas evaluaciones reemplazarían a otros datos sobre toxicidad si la sustancias se encontraran por debajo de los umbrales, o si simplemente sirven como una eficiente asignación de prioridades para la evaluación de riesgos. Hasta ahora, la Comisión Europea (CE) [7] y el Comité Mixto de Expertos FAO / OMS en Aditivos Alimentarios (JECFA) [8] han adoptado el concepto de TTC únicamente para la regulación de sustancias aromatizantes. La aplicación del TTC para FCMs permanece bajo debate. En 2011, Koster y col. propusieron un enfoque de TTC para la regulación de sustancias desconocidas que se encuentran en las muestras de alimentos, incluidas las sustancias añadidas no intencionalmente (NIAS), pero una identificación fiable de NIAS y, en particular, de las sustancias genotóxicas, sigue siendo un problema sin resolver [9]. En 2012, la Comisión Técnica de Productos Fitosanitarios (PPR, Plant Protection Products) aprobó un dictamen científico en el que recomienda el UPT para los metabolitos y los productos de degradación de los pesticidas [10]. En cuanto a los productos de consumo, se han hecho propuestas para abstenerse de realizar ensayos de toxicidad basándose en el sistema REACH (sistema de registro, evaluación, autorización y restricción de sustancias químicas (REACH) en base a las evaluaciones de la exposición y el UPT.
- Discusión
La aplicación pendiente del concepto UPT para la evaluación de las sustancias en contacto con alimentos no evaluadas previamente, requiere un estudio minucioso del rigor y de la idoneidad científicos del concepto. Se plantean seis cuestiones de gran importancia:
- – La evaluación con el UPT se basa en el análisis estructural y en semejanzas químicas. El análisis se basa en los productos químicos que previamente han sido evaluados toxicológicamente, pero la evaluación de un nuevo producto químico puede no requerir datos de toxicidad a menos que se superen los umbrales. ¿Deberían ser evaluados los productos químicos basándose únicamente en similitudes estructurales, y en ausencia de datos sobre su toxicidad?
- – Los valores de UPT provienen de los datos toxicológicos. Se han utilizado gran variedad de factores de incertidumbre y modelos para la extrapolación, a partir de conjuntos de datos toxicológicos de ensayos con animales, de los umbrales de exposición humana en general. ¿Se han evaluado rigurosamente los datos existentes, y se utilizaron los modelos apropiados para obtener los umbrales?
- – El concepto UPT permite evaluar sustancias de estructura química conocida y con datos de exposición conocidos, en ausencia de datos toxicológicos. Sin embargo, para muchas sustancias en contacto con alimentos añadidas no intencionalmente se desconocen los datos sobre su estructura y exposición. ¿Es aplicable el concepto UPT a un número relevante de productos químicos? ¿Cómo abordamos esas sustancias cuya estructura química y / o cuyos datos de exposición se desconocen?
- – Algunos hallazgos científicos recientes en relación con los disruptores endocrinos (EDC, endocrine disrupting chemicals), la toxicidad de las mezclas y las curvas de dosis-respuesta no monotónicas (NMDR) aún no se han incluido con éxito en las evaluaciones de riesgo tradicionales. También representan un reto para una aplicación eficaz del concepto de UPT. ¿Cómo pueden incluirse en el concepto UPT los descubrimientos más recientes en toxicología, una vez que la evaluación de riesgos tradicional encuentre la manera de responder a estas preguntas?
- – Para que las bases de datos reflejen la actualidad científica es necesario incluir continuamente los nuevos datos y avances científicos. Esta forma de proceder puede cambiar los umbrales previamente definidos. ¿Cómo pueden los avances científicos incluirse en las bases de datos de manera eficiente, manteniendo simultáneamente una regulación química fiable y susceptible de aplicación?
- – La aplicación del UPT permite que las sustancias que no excedan los umbrales sean utilizados sin más pruebas toxicológicas. ¿Podría el uso del concepto UPT dar lugar a un estancamiento de los avances toxicológicos?
Leer más
El dossier completo en el que se basa este artículo puede ser recuperado como archivo pdf (en inglés).
5. Referencias
- Rulis, A. (1986). “De minimis and threshold of regulation.” In: Food Protection Technology. C.W. Felix, ed. Lewis Publishers, pp 29-37.
- Munro I.C. et al. (1996). “Correlation of structural class with no-observed-effect levels: a proposal for establishing a threshold of concern.” Food Chem Toxicol 34:829-67.
- Cramer, G. et al. (1978). “Estimation of toxic hazard – a decision tree approach.” Food Cosmet Toxicol 16:255-76.
- Kroes, R. et al. (2000). “Threshold of toxicological concern for chemical substances present in the diet: a practical tool for assessing the need for toxicity testing.” Food Chem Toxicol 38:255-312.
- Kroes, R. et al. (2004). “Structure-based thresholds of toxicological concern (TTC): guidance for application to substances present at low levels in the diet.” Food Chem Toxicol 42:65-83.10.
- EFSA (2012). “Scientific Opinion on exploring options for providing advice about possible human health risks based on the concept of Threshold of Toxicological Concern (TTC).” EFSA Journal 2012;10(7):2750.
- EC (2000). “Commission Regulation (EC) No 1565/2000 of 18 July 2000 laying down the measures necessary for the adoption of an evaluation programme in application of Regulation (EC) No 2232/96 of the European Parliament and of the Council.”
- Munro IC et al. (1999). “A procedure for the safety evaluation of flavouring substances. Joint FAO/WHO Expert Committee on Food Additives.” Food Chem Toxicol 37:207-32.
- Koster, S. et al. (2011). “Application of the TTC concept to unknown substances found in analysis of foods.” Food Chem Toxicol 49:1643-60.
- EFSA (2012). “Scientific Opinion on evaluation of the toxicological relevance of pesticide metabolites for dietary risk assessment.”